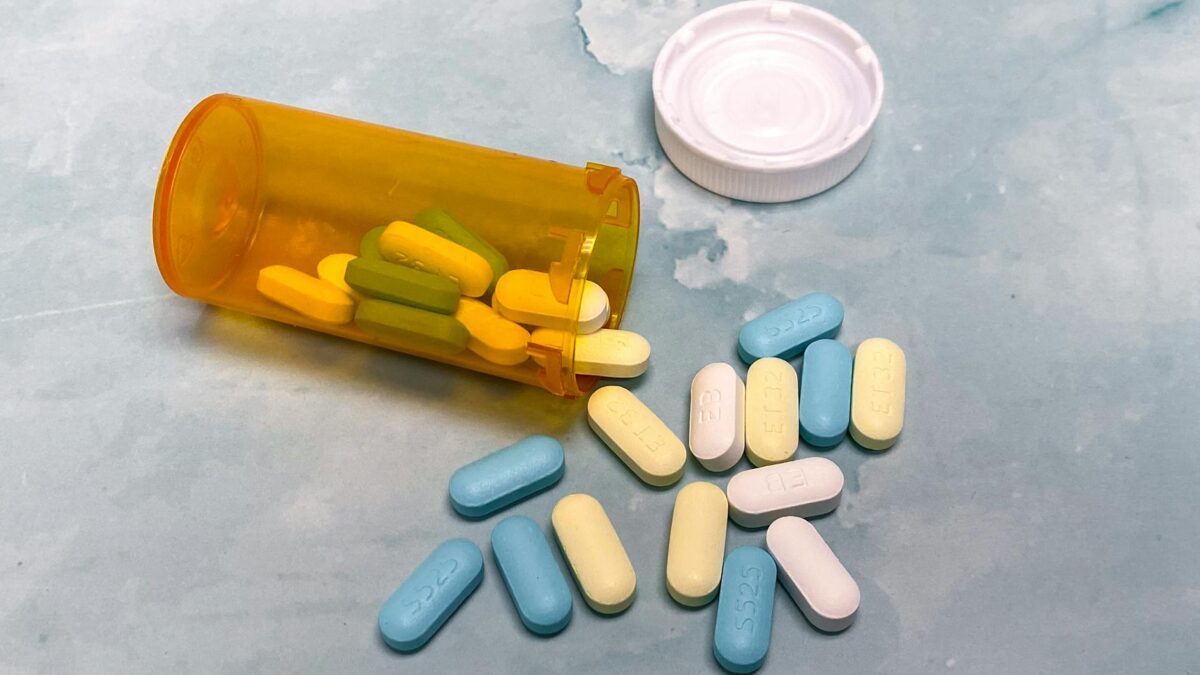
Autoritatea americană pentru medicamente FDA a aprobat vineri primul medicament dedicat unei complicații severe și rare care poate apărea după transplantul de celule stem, disponibil pentru adulți și copii de peste doi ani. Medicamentul vizează microangiopatia trombotică asociată transplantului, o condiție care poate pune în pericol viața pacienților.
Decizia FDA marchează un pas important pentru pacienții care au nevoie de transplant de celule stem, potrivit presei internaționale. După ani de cercetare și o respingere anterioară, acest tratament oferă noi speranțe pentru gestionarea unei complicații care afectează sistemul vascular.
Ce este microangiopatia trombotică asociată transplantului
Microangiopatia trombotică asociată transplantului este o complicație rară dar gravă care se poate dezvolta după transplantul de celule stem hematopoietice. Această condiție afectează vasele de sânge mici, provocând formarea de cheaguri care pot bloca circulația sanguină în organe vitale.
Simptomele includ anemie, scăderea numărului de trombocite și afectarea funcției renale. Fără tratament adecvat, această complicație poate deveni fatală în câteva săptămâni sau luni de la apariție.
Primul medicament aprobat oficial
Până în prezent, pacienții cu această complicație nu aveau acces la un tratament specific aprobat oficial. Medicii foloseau terapii experimentale sau adaptau alte tratamente, cu rezultate variabile și adesea nesatisfăcătoare.
Noul medicament a trecut prin mai multe faze de testare clinică, demonstrând eficacitatea în stabilizarea parametrilor hematologici și îmbunătățirea supraviețuirii pacienților. Tratamentul poate fi administrat atât adulților cât și copiilor cu vârsta de peste doi ani, extindând opțiunile terapeutice pentru o gamă largă de pacienți.
Impact pentru pacienții români
Deși aprobarea FDA se aplică inițial pe piața americană, această decizie poate accelera procesul de autorizare și în Europa, inclusiv în România. Agenția Europeană a Medicamentului evaluează de obicei rapid tratamentele deja aprobate de FDA pentru condiții rare.
În România, transplanturile de celule stem se realizează în centre medicale specializate din București, Cluj-Napoca și Târgu Mureș. Pacienții români care dezvoltă această complicație sunt în prezent tratați cu protocoale adaptate din ghidurile internaționale.
Următorii pași în procesul de aprobare
Compania producătoare va trebui să depună acum dosarul pentru autorizarea medicamentului în Europa. Procesul poate dura între 12 și 18 luni, în funcție de complexitatea evaluării și de răspunsurile la eventualele solicitări de clarificări.
Medicamentul va fi disponibil inițial în spitale și centre de transplant specializate, sub supravegherea directă a hematologilor cu experiență în transplantul de celule stem. Costurile tratamentului nu au fost încă comunicate oficial, dar se estimează că va fi inclus în programele de rambursare pentru boli rare.